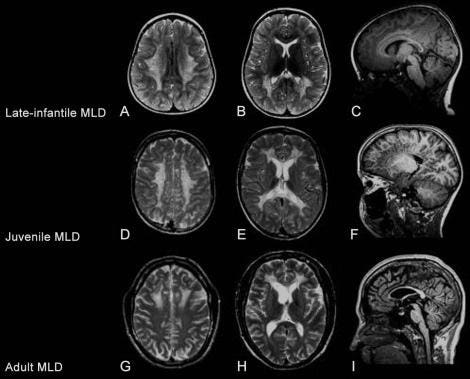
Gambar MR dari tiga pasien dengan MLD
Yu, C. (2017). Gangguan penyimpanan lisosom: sfingolipidosis, bab 10. Biomarker dalam kesalahan metabolisme bawaan. Amsterdam: Elsevier, 211-33.
Cerita ini merupakan bagian dari serangkaian perkembangan dalam Regeneratif Medicine. Pada tahun 1999, saya mendefinisikan regeneratif medicine sebagai kumpulan intervensi yang memulihkan jaringan dan organ yang rusak oleh penyakit, terluka oleh trauma, atau aus oleh waktu ke fungsi normal. Saya termasuk spektrum penuh obat berbasis kimia, gen, dan protein, terapi berbasis sel, dan intervensi biomekanik yang mencapai tujuan tersebut.
Dalam subseri ini, kita fokus secara khusus pada terapi gen. Kita mengeksplorasi perawatan saat ini dan menguji kemajuan yang siap mengubah dunia kesehatan. Setiap artikel dalam koleksi ini membahas aspek berbeda dari peran terapi gen dalam narasi yang lebih besar dari Regeneratif Medicine.
Dalam kedokteran modern, terapi gen telah membuka pintu baru, terutama untuk kondisi yang disebabkan oleh faktor genetik. Leukodistrofi metakromatik, MLD singkatnya, adalah penyakit neurodegeneratif langka namun sangat mengganggu. Hal ini patut diperhatikan karena kesulitannya dan janji potensial dari penelitian terbaru mengenai pengobatan dan kemungkinan penyembuhannya.
Publikasi terbaru di Molecular Therapy menyajikan evaluasi dosis-respons yang mengagumkan dari terapi gen intravena dalam model tikus simtomatik MLD. Studi ini adalah lompatan besar ke depan, memperlihatkan potensi besar dari strategi intervensi genetik untuk melawan dan mungkin membalikkan efek mengganggu dari MLD.
Apakah Metachromatic Leukodystrophy?
Leukodistrofi metakromatik adalah gangguan genetik langka yang mempengaruhi sistem saraf. Kondisi ini disebabkan oleh kekurangan enzim lisosom arilsulfatase A (ARSA), yang memecah sulfatida dalam tubuh. Ketika kadar ARSA rendah, sulfatida menumpuk dalam tubuh dan menyebabkan demielinasi progresif sistem saraf pusat dan perifer.
MLD menyebabkan berbagai gejala, seperti kekakuan otot, kelemahan, kejang, fungsi kognitif terganggu, dan kehilangan penglihatan. Tingkat keparahan gejala dan usia onset mengkategorikan MLD menjadi tiga tipe: infantil akhir, juvenil, dan dewasa. Sayangnya, saat ini belum ada obat untuk penyakit ini. Namun, pengobatan seperti terapi penggantian enzim dan transplantasi sel punca hematopoietik dapat membantu meringankan gejala dan memperlambat perkembangan penyakit. Baru-baru ini, studi telah difokuskan pada pilihan pengobatan untuk terapi gen.
Terapi Gen di Cakrawala
Studi ini memperkenalkan virus terkait adeno yang baru bernama PHP. eB (vektor AAVPHP.eB) yang membawa enzim ARSA. Vektor ini telah menunjukkan hasil yang menjanjikan dalam mengobati penyakit ini dalam model tikus. Pendekatan terapi gen telah memperbaiki anomali penyimpanan sulfatida. Ini memiliki potensi untuk mentransduksi secara luas di pusat saraf dan organ perifer.
Representasi grafis dari studi ini
© 2024 Audouard, E., Khefif, N., Mansat, C., Nelcha, O., Banchi, E. G., Lupiet, C., … & Piguet, F.
Dalam studi ini, para peneliti menggunakan analisis PCR kuantitatif untuk mengukur dengan cermat jumlah salinan genom vektor di berbagai jaringan. Pendekatan mereka memungkinkan mereka untuk menentukan kemampuan transfer gen vektor yang sukses, terutama di area kritis seperti otak dan sumsum tulang belakang, yang sering sulit ditargetkan dengan terapi tradisional. Temuan tersebut menunjukkan bahwa vektor dapat mentransfer gen dengan efisien ke area-area ini, tanda yang menjanjikan untuk aplikasi terapeutik di masa depan.
Signifikansi Studi Ini
Studi ini merupakan langkah signifikan menuju menerjemahkan terapi gen dari model-model teoretis dan studi pra-klinis menjadi jalur perawatan yang klinis dapat diandalkan untuk MLD. Dengan memperlihatkan perbaikan efektif penyimpanan sulfatida di otak dan sumsum tulang belakang melalui rute administrasi non-invasif, penelitian ini membuka pintu baru untuk menangani bukan hanya MLD tetapi juga mungkin penyakit neurodegeneratif dan penyimpanan lisosom lainnya.
Lebih lanjut, aplikasi PCR kuantitatif dalam konteks ini sangat berharga untuk menilai efisiensi transfer gen, menawarkan wawasan yang dapat menyempurnakan dan meningkatkan upaya terapi gen di masa depan. Pendekatan ini memperkuat pemahaman kita tentang dinamika terapi gen. Ini membuka jalan untuk intervensi terapeutik yang lebih tepat dan disesuaikan.
Melampaui hasil yang segera, implikasi lebih luas studi ini memicu anticipasi dan harapan. Ini mendorong bidang terapi gen maju, menyajikan templat yang dapat merevolusi pengobatan penyakit neurodegeneratif dan genetik. Dengan menggabungkan inovasi strategis, ketat ilmiah, dan aplikabilitas praktis, penelitian ini menyajikan bagaimana tantangan yang dihadapi oleh penyakit langka seperti MLD bisa memicu solusi berpionir yang meluas jauh di luar cakupan awalnya.
Langkah Menuju Perawatan Suntikan Langsung
Salah satu kelemahan atau hambatan utama untuk penggunaan terapi modifikasi sel untuk kanker, penyakit autoimun, dan terapi gen adalah kebutuhan akan penggunaan sel autolog. Banyak pengobatan yang dijelaskan hari ini memerlukan isolasi sel target dari individu, menumbuhkannya dalam kultur, memodifikasinya melalui manipulasi gen, pra-pemberian pengobatan pada pasien, dan memasukkan kembali sel yang telah diubah ke dalam pasien. Ablasi imun biasanya diperlukan untuk memungkinkan implantasi sel yang dimodifikasi. Namun, prosedur ini rumit, memakan waktu, mahal, dan terkadang berisiko. Dalam beberapa kasus, abalasi imun menimbulkan bahaya bagi pasien.
Kelemahan ini membuat bottleneck yang parah dalam mengadopsi terapi sel dan terapi gen semacam itu. Laporan ini menawarkan setidaknya sedikit harapan bahwa suntikan langsung dari metode kontrol modifikasi sel tertentu dapat mengatasi keterbatasan ini dan mungkin mengatasi batasan keterbatasan untuk reimplantasi sel autolog. Sebuah vektor modifikasi disuntikkan langsung ke dalam hewan untuk efek yang menguntungkan. Tidak ada keharusan untuk injeksi menjadi autolog. Vektor ini tampaknya menargetkan sel yang tepat secara efektif pada hewan.
Dalam esai yang akan datang untuk Inside Precision Medicine, saya menyoroti signifikansi injeksi langsung sebagai fokus utama dalam terapi modifikasi sel. Metode ini telah menarik perhatian yang besar di berbagai laboratorium penelitian di seluruh dunia, menunjukkan potensi untuk injeksi yang secara mandiri.
Dasar Baru dalam Pengobatan MLD
Misi eksploratif evaluasi dosis-respons ini menandakan perubahan pendekatan kita dalam mengelola MLD dan gangguan genetik serupa. Sementara jalan menuju aplikasi klinis masih dipenuhi dengan tantangan—mulai dari hambatan regulasi hingga kebutuhan akan studi keefektifan dan keamanan yang lebih luas—dasar yang diletakkan oleh penelitian ini menginspirasi pandangan optimis dengan hati-hati.
Penyatuan potensi terapi gen dengan metode administrasi yang praktis, ramah pasien, menggambarkan era baru dalam mengobati kondisi genetik kompleks. Saat kita berdiri di ambang kemajuan medis semacam itu, semangat kolaboratif para peneliti, klinisi, dan pasien tanpa ragu menjadi kunci dalam mengubah wawasan ilmiah ini menjadi manfaat kesehatan yang nyata. Pengejaran inovasi kita secara kolektif, yang didukung oleh studi seperti ini, menyinari jalan menuju masa depan di mana penyakit genetik tidak lagi menentukan kehidupan, tetapi menjadi aspek yang dapat dikelola dalam kehidupan.
Untuk belajar lebih lanjut tentang regeneratif medicine, baca lebih banyak cerita di www.williamhaseltine.com